一、GCP机构简介:
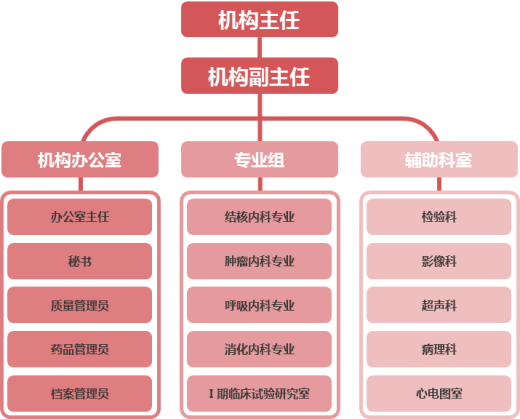
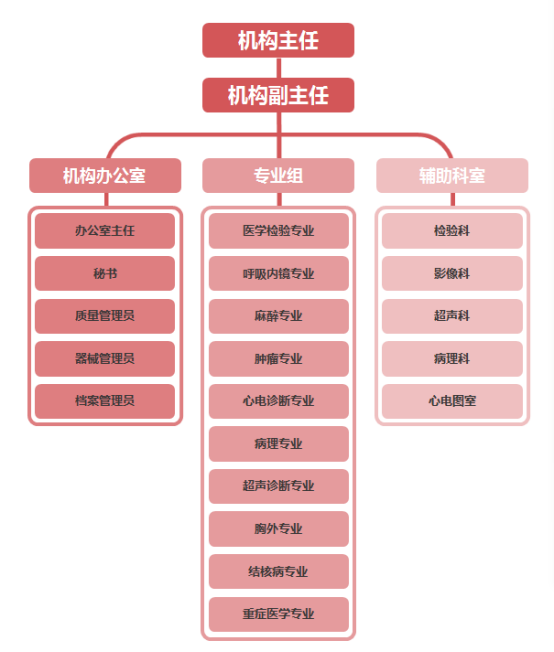
西安市胸科医院药物/医疗器械临床试验机构,于2018年7月通过国家药品监督管理局的严格核查认定并下发GCP认证证书(证书编号:917)。机构下设结核内科、肿瘤内科、呼吸内科、消化内科和I期临床试验研究室等5个药物临床试验专业组,以及医学检验学等10个医疗器械临床试验专业组。各专业组研究团队不仅具有丰富的临床实践经验,而且具备高度的责任心和强大的执行力,始终坚守国家法律法规和伦理规范。
机构依托西安市胸科医院先进的医疗设备,丰富的诊查项目,舒适的就医环境,可靠的急救措施,确保各项检查结果准确,数据均可溯源,受试者的生命安全和权益得以充分保障,全完满足开展各类临床试验的需求。
机构定期对全体研究人员进行GCP培训与考核,确保临床试验不仅科学、合理,更符合伦理和法律的要求。自机构成立以来,我们持续完善制度,修订SOP,健全质量控制和质量保证体系,同时不断优化办事流程,进一步提升研究水平和效率。
通过多年与国内外众多知名制药企业和研究机构的深度合作,不仅验证了我们的试验质量,也为我们赢得了广泛的认可。我们始终秉承“勤谨、仁和、精诚、博新”的理念,致力于提供卓越的临床试验服务。我们热忱欢迎国内外新药研发单位前来考察洽谈,共谋合作,推进医药产业的发展,为人类健康事业贡献力量。
GCP机构办公室电话/传真:029-62500387
接待时间:工作日上午8:00-12:00,下午2:00-5:00
地址:陕西省西安市长安区航天大道东段西安市胸科医院科研楼一层
二、伦理委员会
西安市胸科医院医学伦理委员会成立于2010年,下设4个分委会,其中,临床试验伦理分委会负责对以注册为目的的药物和医疗器械(包括诊断试剂)临床研究及上市后医疗产品进行评价、伦理审查和跟踪。临床试验分委会设有主任委员1名、副主任委员2名,委员10名,专职伦理秘书1人,包括医学、药学、法学、新闻学等专业背景,院外委员2人。
根据我国《药物临床试验质量管理规范》(2020年)、《药物临床试验伦理审查工作指导原则》(2010年)、《医疗器械临床试验质量管理规范》(2022年)、《涉及人的生命科学和医学研究伦理审查办法》(2023年)的要求,委员会对本院进行的涉及人的药物和医疗器械的临床试验进行伦理审查和监督,其宗旨是保护参加临床试验的受试者的尊严、权益和安全,提升生物医学研究的科学性和伦理合理性。
伦理委员会办公室电话:029-62500369(传真)
地址:陕西省西安市长安区航天大道东段西安市胸科医院科研楼3楼。